Streszczenie
Związki halucynogenne kojarzone są przede wszystkim z ich rekreacyjnym przyjmowaniem. Jednakże informacje zarówno na temat mechanizmu działania, jak i właściwości farmakologicznych halucynogenów są znacznie mniej rozpowszechnione.
Większość dotychczasowych badań skupiała się na spektakularnym działaniu związków
halucynogennych, pomijając ich interesujące właściwości uzyskiwane poprzez zastosowanie
niższych dawek, tzw. mikrodawkowanie. Obecnie obserwuje się nawrót zainteresowań
związkami halucynogennymi w zastosowaniach medycznych, o czym świadczy wiele
publikacji naukowych. Daje to nowe światło na podejście do halucynogenów jako związków
mających potencjał terapeutyczny.
Abstract
Hallucinogenic substances are primarily associated with their recreational use. However,
information on both the mechanism of action and the pharmacological properties of
hallucinogens is much less widespread. Up to date, most of the research has focused on
the spectacular effect of hallucinogenic compounds, ignoring their interesting properties
obtained through the use of lower doses, so-called ‘microdosing’. Currently, a renewed
interest in hallucinogenic substances in medical applications is observed, as evidenced by
many articles. This gives a new light to the approach to hallucinogens as compounds with
a therapeutic potential.
Historia związków halucynogennych
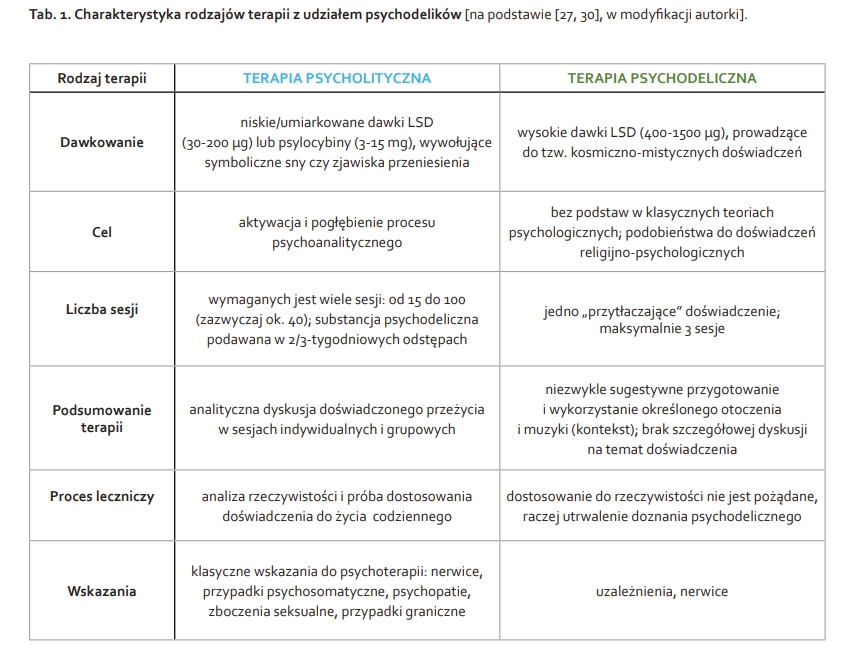
Związki halucynogenne towarzyszą człowiekowi od zarania dziejów, o czym świadczą pozostałości po malowidłach jaskiniowych. Znaleziska z epoki neolitu (3000 lat p.n.e.) potwierdzają używanie substancji narkotycznych do różnych celów. W 2008 r. na wyspie Carriacou (Grenada) archeologowie odkryli akcesoria (miski) datowane na 400 lat p. n. e., służące do przyjmowania związków halucynogennych. Ludzie obcując z przyrodą nauczyli się wykorzystywać związki zawarte w roślinach nie tylko do obrzędów religijnych, ale także do celów leczniczych związanych z medycyną naturalną. Zaobserwowali oni bowiem, że pewne rośliny posiadają właściwości przeciwbólowe czy przeciwlękowe [19]. Chociaż halucynogeny są stosowane w rytuałach religijnych wielu kultur od prawie 2500 lat, w dużej mierze pozostały nieznane społeczeństwu Zachodu aż do okrycia psychoaktywnych własności LSD w 1943 r. Odkrycie to jest dziełem pracy wybitnego szwajcarskiego chemika Alberta Hofmanna (1906–2008), zwanego „ojcem LSD”. Pracując w laboratorium firmy Sandoz podejmował on próby znalezienia związków o właściwościach leczniczych, stymulujących układ oddechowy i układ krążenia. Związkami wyjściowymi były alkaloidy sporyszu, szczególnie ergotamina. W 1938 r. Hofmann zsyntetyzował 25. związek z tej serii, czyli dietyloamid kwasu lizergowego (LSD– 25). Przypadkowe przyjęcie LSD–25 dało początek nowemu kierunkowi badań z zastosowaniem substancji wpływających na świadomość [5, 21]. Początkowo badania wykorzystywały LSD w charakterze psychomimetyku, czyli związku wywołującego objawy psychotyczne zbliżone do schizofrenii. Paradygmat ten był podstawą pierwszych eksperymentów z LSD. Opisywane przez badaczy doświadczenia charakteryzowały się negatywnym podejściem do doznań psychodelicznych [47]. Z pierwotnego modelu psychotomimetycznego wyłoniły się dwa nowe paradygmaty. Oba oparte były na terapii, a nie na obiektywnych opisach działania leku. W końcu pojawiły się dwa różne rodzaje terapii: terapia psycholityczna i terapia psychodeliczna, różniące się przede wszystkim czasem trwania, dawką związku oraz procesem leczniczym. Terapia psycholityczna opiera się na stosowaniu niskich dawek związków psychodelicznych w ciągu kilkunastu sesji, połączonych z dyskusjami na temat przeżytych doświadczeń. Natomiast terapia psychodeliczna wykorzystuje wysokie dawki psychodeliku przyjmowane w odpowiednim otoczeniu w ciągu maksymalnie 3 sesji, bez etapu analizy przeżytych doznań. Szczegółową charakterystykę obu terapii przedstawiono w Tab. 1 [27]. Terapie te stosowane są do dzisiaj i mają na celu wspomaganie procesu leczniczego.
W 1947 r. została opublikowana pierwsza praca kliniczna wskazująca na możliwe zastosowanie LSD w psychiatrii [5]. Do połowy lat 60. ponad 40 000 pacjentów przyjęło LSD, a badania z wykorzystaniem psychodelików doprowadziły do powstania ponad 1000 artykułów naukowych i wielu książek, a także stały się przedmiotem kilku konferencji międzynarodowych. LSD było ważnym narzędziem w neuronauce i opracowywaniu leków, a także wpłynęło na sztukę i społeczeństwo. W latach 50. i 60. XX wieku badano LSD i terapię wspomaganą LSD pod kątem złagodzenia lęku towarzyszącemu terminalnym stadiom nowotworów, w uzależnieniach od alkoholu, zaburzeniach wywołanych używaniem opioidów i w depresji [28]. XX wiek przyniósł wiele odkryć związanych z izolacją, identyfikacją i syntezą związków halucynogennych, takich jak meskalina, N,N– dimetylotryptamina (DMT), fencyklidyna (PCP), ibogaina, psylocybina, ketamina czy wspomniane już LSD [46]. Niestety, zainteresowanie związkami psychoaktywnymi przeniosło się na ich rekreacyjne stosowanie, szczególnie w kręgach kultury hipisowskiej. Wzrastające zainteresowanie znalazło swój finał w otwartej „Wojnie z narkotykami” (ang. War on Drugs) zapoczątkowanej przez prezydenta Stanów Zjednoczonych Richarda Nixona. W 1970 r. rząd amerykański dokonał ponownej klasyfikacji psychodelików i umieścił je w I grupie substancji kontrolowanych, niemających zastosowania medycznego i o dużym ryzyku nadużyć. W rezultacie finansowanie stało się trudniejsze, a badania zostały wstrzymane. Lata 70. i 80. zostały określne mianem „średniowiecza dla badań nad psychodelikami”. Podejście organów władzy do tematyki związków psychoaktywnych miało ogromny wpływ na postrzeganie tych związków przez ludzi niezwiązanych ze światem naukowym [25]. Mimo wielu obiecujących wyników, w ciągu kolejnych 30 lat wokół tematyki związków psychoaktywnych narosło wiele negatywnych emocji. Dodatkowo szerzące się nadużywanie związków halucynogennych i psychostymulantów, przy jednoczesnej walce z ich nielegalną sprzedażą, spowodowały całkowite zdemonizowanie tematu. Badania wznowiono ponownie w XXI wieku.
W ciągu ostatniej dekady pojawiło się wiele wyników wskazujących na istnienie potencjału terapeutycznego związków takich jak psylocybina, ketamina czy LSD [8].
Czym są psychodeliki i jaki jest ich mechanizm działania?
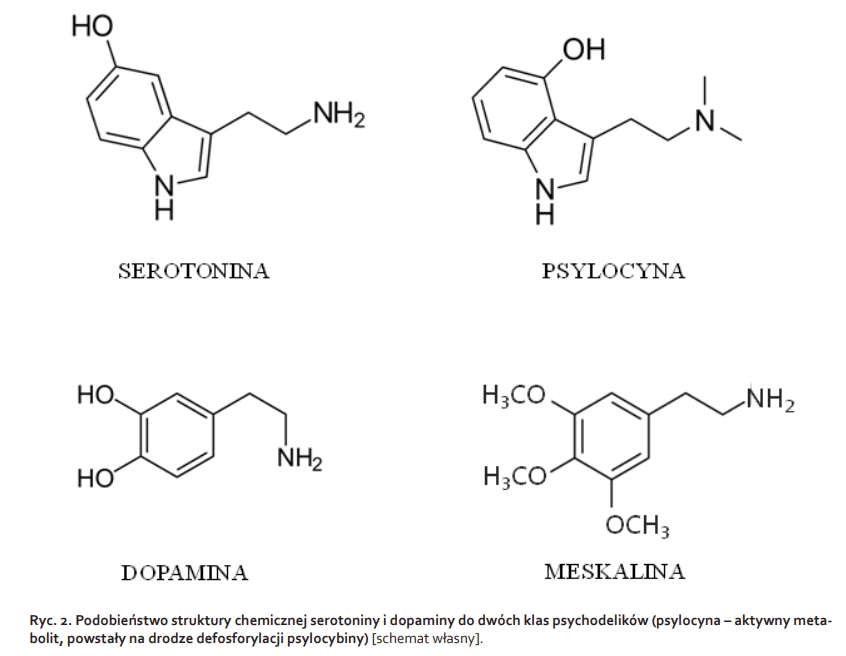
Psychodeliki (halucynogeny serotoninergiczne) są zróżnicowaną grupą związków. Pomimo różnej struktury chemicznej i prawdopodobnie z udziałem różnych mechanizmów molekularnych, wytwarzają podobne zmiany w percepcji, nastroju, procesach poznawczych, sposobie myślenia czy też odczuwania emocji. Nie powodują one jednak uzależnienia fizycznego czy amnezji [15]. Przyjmowanie psychodelików wiąże się z występowaniem halucynacji oraz omamów wzrokowych i słuchowych („widzenie” zapachów, „słyszenie” kolorów, tzw. synestezja), euforii czy depersonalizacji [4]. Niekorzystnym efektem stosowania halucynogenów jest występowanie zjawiska retrospekcji (ang. flashbacks). Obecnie termin ten został zastąpiony bardziej specyficzną nazwą – zaburzenia postrzegania spowodowane halucynogenami (ang. Hallucinogen Persisting Perception Disorder, HPPD). Występowanie HPPD (często kojarzone z przyjmowaniem LSD) związane jest ze zjawiskiem ponownego przeżycia doświadczeń zaistniałych po przyjęciu związku halucynogennego. Wyróżnia się także tzw. „złe podróże” (ang. bad trips), charakteryzujące się poczuciem utraty kontroli nad sytuacją, strachem i myślami samobójczymi [36]. Do negatywnych, krótkotrwałych objawów przyjęcia związków halucynogennych należą: przyspieszenie akcji serca (tachykardia), nieostre widzenie, zawroty głowy, bezsenność, utrata apetytu, suchość w ustach, pocenie się, szybkie zmiany emocjonalne (ze strachu w euforię), impulsywność, obrzęk stóp, dłoni, twarzy, osłabienie i drgawki. Natomiast ciężkie zatrucia oraz długotrwałe przyjmowanie mogą skutkować zapoczątkowaniem psychoz, depresji czy występowania urojeń paranoidalnych [4]. Termin „psychodeliki” w 1957 r. wprowadził brytyjski psychiatra Humphrey Osmond. Słowo to powstało z połączenia dwóch greckich słów psyche (dusza) i delos (ujawnić, objawić) [24]. Pod względem chemicznym związki halucynogenne mogą być zaliczane do dwóch podstawowych klas: pochodnych fenyloalkiloamin i pochodnych indoloalkiloamin, jak przedstawiono na Ryc. 1. W większości związki z grupy indoloalkiloamin swoją budową przypominają neuroprzekaźnik serotoninę, nazywaną „hormonem szczęścia”, natomiast związki z grupy fenyloalkiloamin – neuroprzekaźnik dopaminę (Ryc. 2) [2].
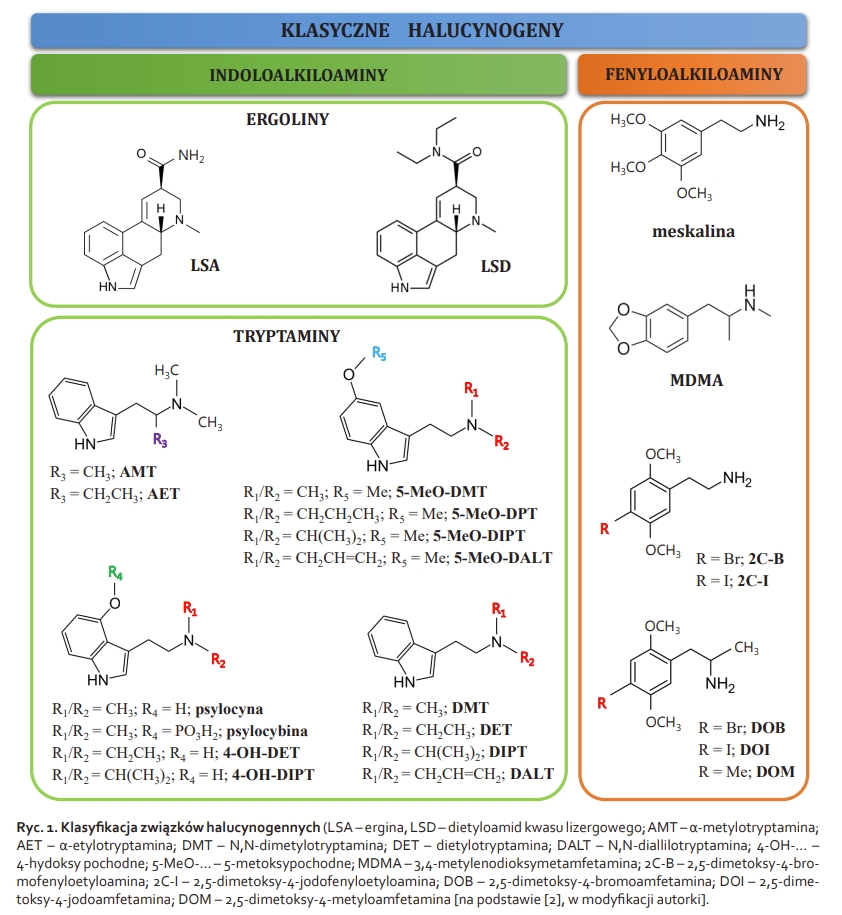
Jednakże halucynogeny są bardzo heterogenną grupą związków, oddziałującą na różne układy neuroprzekaźnikowe, np. układ dopaminergiczny czy glutaminianergiczny. Budowa fenyloalkiloamin opiera się na szkielecie fenyloetyloaminy, która jest dominującą strukturą w szeregu związków endogennych, w tym neuroprzekaźników dopaminy i noradrenaliny. Klasa ta zawiera w sobie pochodne fenyloetyloaminy, a także pochodne fenyloizopropyloaminy (czyli amfetaminy). Przedstawicielami podgrupy fenyloetyloamin jest meskalina (alkaloid występujący w kaktusach peyote) czy syntetyczny związek 2,5–dimetoksy–4–jodofenyloetyloamina (2C–I). Natomiast do amfetamin zaliczamy np. 2,5–dimetoksy–4–jodoamfetaminę (DOI) oraz 3,4–metylenodioksymetamfetaminę (popularne MDMA) (Ryc. 1). W klasie indoloalkiloamin można wyróżnić 2 podgrupy: proste tryptaminy (np. psylocybinę czy DMT) oraz ergoliny (LSD) (Ryc. 1). Różnego rodzaju modyfikacje cząsteczki tryptaminy przyczyniają się do powstawania nowych związków o rozmaitych właściwościach chemicznych, które w konsekwencji mają zdolność indukowania odmiennych stanów umysłu i zachowań. Fenyloalkiloaminy są najczęściej badaną klasą psychodelików ze względu na ich stosunkowo łatwą syntezę [2, 33].
Zasadniczo mechanizm działania psychodelików związany jest z ich wysokim powinowactwem do receptorów serotoninowych (ang. 5-hydroxytryptamine receptor, 5–HTR), szczególnie 5–HT1A i 5–HT2A/2C. Związki te są agonistami (aktywatorami) lub częściowymi agonistami receptorów serotoninowych. Wyróżnia się 7 rodzin receptorów serotoninowych (od 5–HT1 R do 5–HT7 R), a każda rodzina składa się z kilku podtypów. Receptory z rodziny 5–HT2 (np. 5–HT2A i 5–HT2C) są receptorami pobudzającymi, zaś receptory z rodziny 5–HT1 (np. 5–HT1A) to receptory hamujące. Receptory serotoninowe są receptorami metabotropowymi sprzężonymi z białkami G (oprócz rodziny 5–HT3 ,które są kanałami jonowymi) [36, 37]. Aktywacja receptora 5–HT2A związana jest z działaniem halucynogennym psychodelików. Receptory 5– HT2A występują korze mózgowej, wzgórzu, miejscu sinawym (LC, łac. locus coeruleus) czy polu brzusznym nakrywki (VTA, łac. area tegmentalis ventralis). Należy wspomnieć o równie istotnym zaangażowaniu receptora 5–HT1A w mechanizm działania psychodelików. Jest to szczególnie ważne w przypadku tryptamin i LSD, które na ogół wykazują znaczące powinowactwo do tego podtypu receptora serotoninowego. Badania wykazały, że receptory 5–HT1A współwystępują z receptorami 5–HT2A na komórkach piramidowych kory mózgowej. Wykazują jednak przeciwny efekt niż receptory 5–HT2A, związany z ich hamującym charakterem. Receptory 5–HT1A zlokalizowane presynaptycznie na ciałach neuronów w jądrach szwu (tzw. autoreceptory) osłabiają uwalnianie serotoniny z tej struktury. Oprócz tego ich największą gęstość odnotowano w obszarach limbicznych, np. w hipokampie. Z kolei wyższe dawki związków halucynogennych pobudzają receptory 5–HT2C. Aktywacja tych receptorów często funkcjonalnie przeciwdziała efektom pobudzenia receptora 5–HT2A, gdyż w większym stopniu receptory 5–HT2C zlokalizowane są na interneuronach GABAergicznych i powodują uwalnianie tego hamującego neuroprzekaźnika (GABA, kwas γ–aminomasłowy). Tak więc sumaryczny efekt psychodelików jest wypadkową pobudzenia wszystkich 3 podtypów receptora serotoninowego i ich modulującego efektu zależnego od lokalizacji. Ciała neuronów serotoninowych zlokalizowane są głównie w grzbietowej części jąder szwu (RN, łac. nuclei raphes), skąd wysyłane są projekcje do korowych i limbicznych (związanych z emocjami) rejonów mózgu. Mechanizm działania psychodelików może polegać na stymulowaniu różnych struktur mózgowych za pośrednictwem receptorów serotoninowych, które są przez te substancje pobudzane.
Lokalizacja receptorów 5–HT1A, 5–HT2A i 5–HT2C sprawia, że wykazują one „rozproszony” wpływ na wiele szlaków neuronalnych, a tym samym oddziałują na różne funkcje ośrodkowego układu nerwowego. Zarówno fenyloalkiloaminy, jak i indoloalkiloaminy powodują pobudzenie receptorów 5–HT2A. Jednakże w przypadku drugiej klasy efekt ten jest pośredni, z udziałem transportera serotoninowego SERT. Zadaniem SERT jest wychwyt zwrotny serotoniny z przestrzeni synaptycznej do zakończenia nerwowego. W wyniku hamowania SERT dochodzi do zwiększenia poziomu serotoniny w przestrzeni synaptycznej i w konsekwencji – pobudzenia receptorów 5–HT2A. Natomiast fenyloalkiloaminy stymulują receptor 5–HT2A (do którego wykazują największe powinowactwo) w sposób bezpośredni. Stymulacja 5–HT2AR powoduje uwalnianie glutaminianu (głównego neuroprzekaźnika pobudzającego) z komórek piramidowych. Pobudzenie 5–HT1AR hamuje uwalnianie GABA, doprowadzając do odhamowania komórek piramidowych. Natomiast pobudzenie 5–HT2CRwzmacnia uwalnianie GABA, skutkując hamowaniem aktywności komórek piramidowych. Aktywność komórek piramidowych ma wpływ na szlaki dopaminergiczne i serotoninergiczne, wstępujące odpowiednio z VTA i istoty czarnej (SN, łac. substantia nigra) oraz RN. Zależnie od stopnia stymulacji pobudzającego unerwienia glutaminianergicznego, obserwuje się wzrost lub spadek uwalniania dopaminy i serotoniny z zakończeń w prążkowiu (STR, łac. striatum), jądrze półleżącym przegrody (NAS, łac. nucleus accumbens) i kory czołowej (FCx, łac. frontal cortex). Stopień pobudzenia receptorów 5–HT1A i 5–HT2C, występujących głównie na interneuronach GABAergicznych, wykazuje działanie modulujące w obserwowanym efekcie. Uproszczony mechanizm działania psychodelików przedstawiono na Ryc. 3. Rozpoznanie funkcjonalnego znaczenia wymienionych struktur pomaga zrozumieć złożoną farmakologię związków halucynogennych [36, 40].
Związki halucynogenne w badaniach podstawowych
Podczas doświadczeń laboratoryjnych zaobserwowano bardzo istotne procesy zachodzące pod wpływem halucynogenów. Badania wykazały wzrost ekspresji genów wczesnej odpowiedzi komórkowej (IEG ang. immediate early genes), tj. c-Fos, ngf1c czy arc, po zastosowaniu agonistów receptorów serotoninowych DOI oraz LSD [26, 35, 44]. IEG aktywowane są w sposób szybki i przejściowy, reprezentując stały mechanizm odpowiedzi na różne bodźce komórkowe. Mechanizm ten aktywowany jest na poziomie transkrypcji (przepisywania informacji genetycznej z DNA na RNA), zanim jakiekolwiek inne białka zostaną zsyntetyzowane. Geny te biorą udział między innymi w procesach uczenia się i konsolidacji pamięci, a ich obniżona ekspresja obserwowana jest np. u pacjentów cierpiących na schizofrenię czy zaburzenia depresyjne [16]. Inne badania podkreślają rolę DOI i ketaminy w podwyższaniu poziomu ekspresji czynnika troficznego pochodzenia mózgowego (BDNF, ang. brain derived neurotropic factor). Neutrofiny to małe białka wytwarzane przez układ nerwowy, mające istotny wpływ na funkcjonowanie komórek nerwowych. BDNF jest neutrofiną zaangażowaną w rozwój neuronów, modyfikacje morfologii dendrytów oraz pobudzenie do wzrostu i różnicowania nowych neuronów i synaps [29, 45]. Zaobserwowano, że w hodowlach komórkowych pod wpływem DOI aktywowane są receptory dla neurotrofin oraz następuje proces wydłużania aksonów [32]. Kolejne badania wykazały, że związki halucynogenne takie jak: LSD, DMT oraz DOI wspierają wzrost gałęzi i kolców dendrytycznych oraz stymulują tworzenie nowych połączeń synaptycznych (synaptogenezę) [31]. Wymienione procesy związane są z tzw. plastycznością neuronalną. Termin ten obejmuje takie mechanizmy jak: modyfikacje wewnątrzkomórkowych kaskad sygnałowych, regulację ekspresji genów, zmiany poziomu i liczby połączeń synaptycznych, zmiany w uwalnianiu neuroprzekaźników, a także powstawanie nowych neuronów w określonych obszarach ośrodkowego układu nerwowego. Stąd neuroplastyczność utożsamiana jest z adaptacją układu nerwowego do określonych warunków w organizmie [13]. Co ciekawe, od niedawna wyróżnia się nową klasę związków zdolnych do szybkiego promowania strukturalnej i funkcjonalnej plastyczności neuronalnej, tzw. psychoplastogeny (gr. psych /umysł/ – plast / formować/ – gen /produkować/). Związki psychoplastogenne obejmują związki psychodeliczne (DMT, LSD) i ketaminę [38]. Testy behawioralne przeprowadzone w modelu zwierzęcym wskazują, że LSD i psylocybina mogą być skuteczne w leczeniu depresji [20]. Okazuje się również, że o ile jednorazowe podanie DMT może wywoływać reakcje lękowe, to jego długotrwałe zastosowanie ma tendencję do zmniejszania lęku. Testy behawioralne dowiodły, że DMT u gryzoni wykazuje działanie przeciwdepresyjne oraz przeciwlękowe. Badania te sugerują zasadność stosowania psychodelików w leczeniu depresji oraz zespołu stresu pourazowego (PTSD, ang. post- -traumatic stress disorder) [10].
Ostatnio pojawiły się prace potwierdzające, iż chroniczne stosowanie mikrogramowych dawek psychodelików niewywołujących halucynacji (tzw. mikrodawkowanie) może rzeczywiście wykazywać potencjał terapeutyczny w działaniu przeciwlękowym i przeciwdepresyjnym. Mikrodawkowanie wiąże się z poprawą stanu psychicznego, eliminacją postaw dysfunkcyjnych, otwartością umysłu, wzrostem poczucia wartości i kreatywnością. Badania na modelu szczurzym wykazały, że wielokrotne przerywane podawanie niskich dawek DMT wytwarza fenotyp przeciwdepresyjny i wzmaga proces wyciszania strachu bez wpływu na pamięć roboczą lub interakcje społeczne [9]. Z drugiej strony inni badacze postulują, że podanie ketaminy i psylocyny (aktywnego metabolitu psylocybiny) w paradygmacie mikrodawkowania miało działanie prolękowe [22]. Niemniej jednak przytoczone przykłady dają dużą nadzieję, że związki halucynogenne wpływają pozytywnie na procesy związane z synaptogenezą, neuroplastycznością oraz przywracaniem homeostazy w układzie nerwowym. Są to jednak wyniki badań in vitro (hodowle komórkowe) lub in vivo na modelach zwierzęcych, które wymagają potwierdzenia klinicznego.

Psychodeliki w badaniach klinicznych
Pierwsze próby kliniczne z użyciem LSD rozpoczęły się jeszcze w latach 50. XX wieku. Uzyskane wyniki były bardzo obiecujące. Jednakże późniejsze restrykcje dotyczące badań z wykorzystaniem psychodelików doprowadziły do spadku zainteresowań terapeutycznymi właściwościami związków psychodelicznych i pozostawiły wiele pytań bez odpowiedzi. Ponowne zainteresowanie halucynogenami w XXI wieku zaowocowało wieloma interesującymi badaniami z udziałem ludzi. Psylocybina zastosowana w dawkach umiarkowanych (0,2 mg/kg) wykazała tendencję do poprawy nastroju u pacjentów w zaawansowanym stadium raka [18]. Zastosowanie wysokiej dawki psylocybiny (22–30 mg/70 kg) poprawiło jakość życia pacjentów z rozpoznanym nowotworem złośliwym [17]. Psychodeliki okazały się skuteczne w łagodzeniu klasterowych bólów głowy. Schorzenie to jest rodzajem samoistnego napadowego bólu głowy, występującego okresowo. Etiologia tej choroby nie jest do końca wyjaśniona. W przeprowadzonych badaniach psylocybina hamowała napady bólu, a przyjmowanie psylocybiny i LSD u większości pacjentów całkowicie eliminowało epizody klasterowych bólów głowy oraz wydłużyło okres remisji (okres schorzenia charakteryzujący się brakiem objawów chorobowych) [42]. W kontrolowanym środowisku klinicznym przyjęcie psylocybiny w szerokim zakresie dawek (0.1; 0.2; 0.3 mg/ kg) przez pacjentów cierpiących na zaburzenia obsesyjno-kompulsywne powodowało znaczne zmniejszenie symptomów choroby [34]. Psylocybina okazała się również pomocna w wspomaganiu leczenia uzależnień od nikotyny czy alkoholu. Wykazano, że 80% uczestników badania po piętnastotygodniowym okresie rzucenia palenia papierosów wspomaganego przyjmowaniem psylocybiny (20–30 mg/70 kg) zachowało abstynencję nikotynową przez kolejnych 6 miesięcy [23]. Natomiast osoby uzależnione od alkoholu uczestniczące w dwunastotygodniowym badaniu z czternastoma sesjami psylocybinowymi (0.3; 0.4 mg/kg), utrzymały abstynencję do 36 miesięcy po zakończeniu badania [6]. Psychodeliki znalazły także zastosowanie w leczeniu uzależnienia opioidowego od takich narkotycznych leków przeciwbólowych jak: fentanyl, metadon, buprenorfina czy tramadol oraz od narkotyków, np. morfiny, heroiny. W badaniu z udziałem osób uzależnionych od opioidów uczestnicy przyjmowali ibogainę, pochodną tryptaminy obecną w korze afrykańskiej rośliny Tabernanthe iboga. Ibogaina istotnie zmniejszała objawy odstawienia od opioidów i hamowała głód narkotykowy [7]. Problem kryzysu opioidowego jest szczególnie widoczny w Stanach Zjednoczonych. Psychodeliki znalazły również zastosowanie w terapii lekoopornej depresji. Podanie dwóch dawek psylocybiny w odstępie tygodniowym (10 i 25 mg) spowodowało szybkie i trwałe działanie przeciwdepresyjne [12]. Badania z użyciem rytualnego napoju ayahuasca, w którego skład wchodzi min. DMT, harmina i harmalina, pokazały jego korzystny wpływ na nastrój zdrowych ochotników poprzez osłabienie uczucia lęku, beznadziejności i odczuwania paniki [41]. Alkaloidy ß–karbolinowe: harmina i harmalina (zredukowana, częściowo uwodniona forma harminy) w sposób odwracalny hamują aktywność monoaminooksydazy A (MAO–A), enzymu odpowiedzialnego za rozkład takich neuroprzekaźników jak serotonina, dopamina czy noradrenalina. Związki te można znaleźć w południowoamerykańskich pnączach z rodziny malpigiowatych Banisteriopsis caapi. Natomiast DMT zawarta jest w jednym z gatunków krzewu z rodziny marzanowatych – Psychotria viridis. Samodzielnie przyjęta DMT jest nieaktywna. Dopiero dodatek inhibitorów MAO–A (harminy, harmaliny) zapobiega szybkiemu metabolizmowi DMT i przedłuża jej działanie poprzez ominięcie tzw. efektu pierwszego przejścia. Pozwala to na wystąpienie efektu psychodelicznego [43]. Ponadto pojedyncze spożycie ayahuasca (2 ml/kg) zmniejszyło objawy depresyjne u pacjentów przez okres 14 dni [14]. Badacze z Imperial College London wykazali, że pod wpływem LSD różne rejony mózgu wykazują nasiloną komunikację, która nie występuje w normalnych warunkach. Jednocześnie odnotowano osłabienie standardowej aktywności mózgu (DMN, ang. default mode network), definiowanej jako sieć współdziałających regionów mózgu, która jest nasilona w stanach lękowych [11]. Równie interesujące okazało się porównanie złożoności wzorców funkcjonowania mózgu po psylocybinie w porównaniu do placebo (Ryc. 4). Pod wpływem psylocybiny pojawiło się wiele przejściowych struktur o małej stabilności, których nie obserwuje się w przypadku podania placebo [39].
Istotne jest również odkrycie własności terapeutycznych MDMA u pacjentów z PTSD. Schorzenie to jest następstwem traumatycznego wydarzenia i powoduje anhedonię (brak zdolności odczuwania przyjemności), nawracające lęki i problemy ze snem oraz nieustanne podenerwowanie. Uczestnicy badań klinicznych z użyciem MDMA zauważyli poprawę swojej samoświadomości, relacji i umiejętności społecznych, większą motywację do podejmowania aktywności fizycznej oraz otwartość na kontynuację terapii. Przyjęcie MDMA pozwoliło również na zredukowanie ilości przyjmowanych leków, stosowanych w celu złagodzenia objawów PTSD. Relacje uczestników badania wskazują na wyeliminowanie problemów związanych z nieprawidłowym ciśnieniem tętniczym krwi, odczuwaniem bólu czy występowaniem lęku. Obserwowane u osób cierpiących na PTSD nadużywanie alkoholu oraz nielegalnych substancji, celem niejako ucieczki od lęku, także zostało zredukowane [3]. Zastosowanie mikrodawkowania u ludzi wykazało wiele pozytywnych efektów. Testy z wykorzystaniem np. Brief Wisdom Screening Scale dowiodły, że osoby stosujące mikrodawkowanie uzyskały niższą punktację w pomiarach postaw dysfunkcyjnych (predysponujących do objawów depresji) i negatywnej emocjonalności, natomiast wyższą punktację w odniesieniu do otwartości, mądrości (rozumianej jako zdolności uczenia się na własnych błędach) oraz kreatywności, w porównaniu do osób nie przyjmujących psychodelików. Ankietowani byli w większości użytkownikami LSD (65%) i/lub psylocybiny (28%) [1].
Doświadczenia terapeutów w pracy z pacjentami wykazały, iż przyjmowanie psychodelików może ułatwić zajrzenie „w głąb siebie”, a przez to pomóc w spojrzeniu w inny sposób na otaczające nas problemy. Można przypuszczać, że już pojedyncze podanie związku psychodelicznego spowoduje długotrwałe, pozytywne zmiany behawioralne oraz fizjologiczne, między innymi na poziomie ekspresji genów. Istotnymi składowymi terapii za pomocą psychodelików są: kontekst (otoczenie, muzyka), wsparcie terapeuty oraz dawka związku. Nierozłącznym elementem wspomnianej triady jest proces przygotowań przed sesją oraz proces integracji po sesji psychodelicznej. Proces integracji pozwala na rozpracowanie emocji wywołanych przez związki psychoaktywne oraz na ich konfrontację i połączenie z nowymi doświadczeniami w życiu codziennym [30].

Podsumowanie
W oparciu o wyniki badań klinicznych przypuszcza się, że związki halucynogenne nie są złem koniecznym, a co więcej, mogą posiadać potencjał terapeutyczny w przypadku wspomagania leczenia różnorakich dolegliwości i chorób. Jednakże należy pamiętać, że w tym przypadku przyjmowanie związków psychoaktywnych jest formą terapii, tak więc powinno się odbywać pod ścisłą kontrolą specjalisty. Brak wsparcia psychicznego w przejściu przez doświadczenie psychodeliczne może mieć bardzo negatywne skutki. Przedstawione powyżej obiecujące wyniki badań dotyczące stosowania związków halucynogennych w różnego rodzaju schorzeniach to jedynie część historii dotyczącej tych związków. Temat ten zyskuje na popularności, szczególnie ze względu na potrzebę znalezienia lepszych terapii, obarczonych mniejszym ryzykiem występowania skutków ubocznych i cechujących się większą skutecznością. Jednocześnie należy zaznaczyć, że związki psychodysleptyczne nowej generacji (pochodne LSD, związki serii NBOMe) ze względu na swoją wysoką aktywność farmakologiczną i długi czas działania mogą być niebezpieczne nawet wówczas, gdy są zażywane w mikrogramowych dawkach. Szwajcarscy psychiatrzy Peter Gesser i Peter Oehen posiadają już rządowe licencje na stosowanie psychodelików (LSD, MDMA) w prywatnej praktyce psychoterapeutycznej. Możliwe, że terapeutyczne zastosowanie psychodelików uzyska większą popularność. Nie jest to tak niemożliwe, jakby się mogło wydawać, gdyż cytując Paracelsusa, ojca medycyny nowożytnej – „wszystko jest trucizną i nic nie jest trucizną, bo tylko dawka czyni truciznę”. Kto wie, może gdyby nie utrudnienia w przeprowadzaniu badań sprzed kilkudziesięciu lat, już dzisiaj psychodeliki byłyby częścią standardowej terapii wspomagającej np. w depresji lub innych schorzeniach o podłożu lękowym. Zdecydowanie na ten moment musimy jeszcze poczekać, przeprowadzić wiele dodatkowych badań i podejść do tego tematu z dużą pokorą.
Podziękowania
Monika Herian dziękuje za dofinansowanie w ramach projektu InterDokMed numer POWR.03.02.00– 00–I013/16 oraz grantu Narodowego Centrum Nauki OPUS 11 numer 2016/21/B/NZ7/01131.
Bibliografia
1. Anderson T., Petranker R., Rosenbaum D., Weissman C. R., Dinh–Williams L.–A., Hui K., Hapke E, Farb
N. A. S. (2019). Microdosing psychedelics: personality, mental health, and creativity differences in microdosers. Psychopharmacology, 236:731–740 doi:10.1007/s00213–018–5106–2
2. Araújo A. M., Carvalho F., Bastos M. de L., Guedes de Pinho P., Carvalho M. (2015). The hallucinogenic
world of tryptamines: an updated review. Archives of Toxicology, 89: 1151–1173 doi:10.1007/s00204–
015–1513–x
3. Barone W., Beck J., Mitsunaga–Whitten M., Perl P. (2019). Perceived benefits of MDMA–assisted psychotherapy beyond symptom reduction: qualitative follow–up study of a clinical trial for individuals with
treatment–resistant PTSD. Journal of Psychoactive Drugs, 51:199–208 doi:10.1080/02791072.2019.158
0805
4. Baumann M. H., Glennon R. A., Wiley J. L. (Eds) (2017). Neuropharmacology of New Psychoactive Substances (NPS). Current Topics in Behavioral Neurosciences, vol. 32, Cham, Szwajcaria doi:10.1007/978–
3–319–52444–3
5. Begola M. J., Schillerstrom J. E. (2019). Hallucinogens and Their Therapeutic Use. Journal of Psychiatric
Practice, 25: 334–346 doi:10.1097/pra.0000000000000409
6. Bogenschutz M. P., Forcehimes A. A., Pommy J. A., Wilcox C. E. et al. (2015). Psilocybin–assisted treatment for alcohol dependence: a proof–of–concept study. Journal of Psychopharmacology, 29: 289–299.
doi: 10.1177/0269881114565144
7. Brown T. K., Alper K. (2017). Treatment of opioid use disorder with ibogaine: detoxification and drug
use outcomes. The American Journal of Drug and Alcohol Abuse, 44: 24–36 doi:10.1080/00952990.201
7.1320802
8. Burki T. K. (2020). Psychedelics for alcohol use disorder: state of the research. The Lancet Gastroenterology and Hepatology, 5: 243–244 doi: 10.1016/S2468–1253(20)30024–8
9. Cameron L. P., Benson C. J., DeFelice B. C., Fiehn O. et al. (2019). Chronic, intermittent microdoses of
the psychedelic N,N–dimethyltryptamine (DMT) produce positive effects on mood and anxiety in rodents.
ACS Chemical Neuroscience, 10: 3261–3270 doi:10.1021/acschemneuro.8b00692
10. Cameron L. P., Benson C. J., Dunlap L. E., Olson D. E. (2018). Effects of N,N–dimethyltryptamine on rat
behaviors relevant to anxiety and depression. ACS Chemical Neuroscience, 9: 1582–1590 doi:10.1021/
acschemneuro.8b00134
11. Carhart–Harris R. L., Muthukumaraswamy S., Roseman L., Kaelen M. et al. (2016). Neural correlates of
the LSD experience revealed by multimodal neuroimaging. Proceedings of the National Academy of Sciences, 113: 4853–4858 doi:10.1073/pnas.1518377113
12. Carhart–Harris R. L., Roseman L., Bolstridge M., Demetriou L. et al. (2017). Psilocybin for treatment–resistant depression: fMRI–measured brain mechanisms. Scientific Reports, 7: 13187 doi: 10.1038/s41598–
017–13282–7
13. Citri A., Malenka R.C. (2008). Synaptic plasticity: multiple forms, functions, and mechanisms. Neuropsychopharmacology, 33: 18–41 doi:10.1038/sj.npp.1301559
14. de Lima Osório F., de Macedo L. R. H., de Sousa J. P. M., Pinto J. P. et al. (2011). The therapeutic potential
of harmine and ayahuasca in depression: Evidence from exploratory animal and human studies. W: The
ethnopharmacology of ayahuasca, 75–85. dos Santos R. E. (Ed.) Transworld Research Network, Kerala,
Indie
15. American Psychiatric Association (2013) Diagnostic and Statistical Manual of Mental Disorders: Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition, VA: American Psychiatric Association,
Arlington, USA
16. Gallo F. T., Katche C., Morici J. F., Medina J. H. et al. (2018). Immediate early genes, memory and psychiatric disorders: focus on c–Fos, Egr1 and Arc. Frontiers in Behavioral Neuroscience, 12: 79 doi:10.3389/
fnbeh.2018.00079
17. Griffiths R. R., Johnson M. W., Carducci,M. A., Umbricht A. et al. (2016). Psilocybin produces substantial
and sustained decreases in depression and anxiety in patients with life–threatening cancer: A randomized
double–blind trial. Journal of Psychopharmacology, 30: 1181–1197 doi:10.1177/0269881116675513
18. Grob C. S., Danforth A. L., Chopra G. S., Hagerty M. et al. (2011). Pilot study of psilocybin treatment
for anxiety in patients with advanced–stage cancer. Archives of General Psychiatry, 68: 71 doi:10.1001/
archgenpsychiatry.2010.116
19. Guerra–Doce E. (2015). Psychoactive Substances in Prehistoric Times: Examining the Archaeological
Evidence. Time and Mind, 8: 91–112 doi:10.1080/1751696x.2014.993244
20. Hibicke M., Landry A. N., Kramer H. M., Talman Z. K. et al. (2020). Psychedelics, but not ketamine,
produce persistent antidepressant–like effects in a rodent experimental system for the study of depression.
ACS Chemical Neuroscience, 11: 864–871 doi:10.1021/acschemneuro.9b00493
21. Hofmann A. (1970). Notes and documents concerning the discovery of LSD. Agents and Actions, 1:148–
150 doi: 10.1007/BF01982402
22. Horsley R. R., Páleníček T., Kolin J., Valeš K. (2018). Psilocin and ketamine microdosing: effects of subchronic intermittent microdoses in the elevated plus–maze in male Wistar rats. Behavioural Pharmacology, 29: 530–536 doi:10.1097/fbp.0000000000000394
23. Johnson M. W., Garcia–Romeu A., Cosimano M. P., Griffiths R. R. (2014). Pilot study of the 5–HT2AR
agonist psilocybin in the treatment of tobacco addiction. Journal of Psychopharmacology, 28: 983–
992doi:10.1177/0269881114548296
24. Kaplan R. M. (2016). Humphry Fortescue Osmond (1917–2004), a radical and conventional psychiatrist:
The transcendent years. Journal of Medical Biography, 24: 115–124 doi: 10.1177/0967772013479520
25. Langlitz N. (2012). Neuropsychedelia: The revival of hallucinogen research since the decade of the brain,
University of California Press, Berkeley and Los Angeles, USA
26. Leslie R. A., Moorman J. M., Coulson A., Grahame–Smith D. G. (1993) Serotonin2/1C receptor activation
causes a localized expression of the immediate–early gene c–fos in rat brain: evidence for involvement of
dorsal raphe nucleus projection fibres. Neuroscience, 53: 457–463 doi:10.1016/0306–4522(93)90209–x
27. Leuner H. (1967). Present state of psycholytic therapy and its possibilities. W: The Use of LSD in Psychotherapy and Alcoholism. Abramson, H.A. (Ed.) The Bobbs–Merrill Company, Indianapolis, USA
28. Liechti M. E. (2017). Modern Clinical Research on LSD. Neuropsychopharmacology, 42: 2114–2127
doi:10.1038/npp.2017.86
29. Liu R. J., Lee F. S., Li X. Y., Bambico F. et al. (2012). Brain–derived neurotrophic factor Val66Met allele
impairs basal and ketamine–stimulated synaptogenesis in prefrontal cortex. Biological Psychiatry, 71:
996–1005 doi:10.1016/j.biopsych.2011.09.030
30. Lorenc M. (2019). Czy psychodeliki uratują świat? Wydawnictwo Krytyki Politycznej, Kopyt S. (Ed.),
Warszawa, Polska
31. Ly C., Greb A. C., Cameron L. P., Wong J. M. et al. (2018). Psychedelics promote structural and functional
neural plasticity. Cell Reports, 23: 3170–3182 doi:10.1016/j.celrep.2018.05.022
32. Marinova Z., Walitza S., Grünblatt E. (2017). The hallucinogen 2,5–dimethoxy–4–iodoamphetamine hydrochloride activates neurotrophin receptors in a neuronal cell line and promotes neurites extension. Journal of Neural Transmission, 124: 749–759 doi:10.1007/s00702–017–1706–y
33. Meyerhoefer M. M. (2010). Serotonergic hallucinogens. W: Addiction Medicine. Johnson B. A. (Ed.),
585–602 doi:10.1007/978–1–4419–0338–9_27
34. Moreno F. A., Wiegand C. B., Taitano E. K., Delgado P. L. (2006). Safety, tolerability, and efficacy of psilocybin in 9 patients with obsessive–compulsive disorder. The Journal of Clinical Psychiatry, 67: 1735–
1740 doi:10.4088/jcp.v67n1110
35. Nichols C. D., Sanders–Bush E. (2002). A single dose of lysergic acid diethylamide influences gene expression patterns within the mammalian brain. Neuropsychopharmacology, 26: 634–642 doi:10.1016/
s0893–133x(01)00405–5
36. Nichols D. E. (2016). Psychedelics. Pharmacological Reviews, 68: 264–355 doi:10.1124/pr.115.011478
37. Nichols D. E., Nichols C. D. (2008). Serotonin Receptors. Chemical Reviews, 108: 1614–1641 doi:10.1021/
cr078224o
38. Olson D. E. (2018). Psychoplastogens: a promising class of plasticity–promoting neurotherapeutics. Journal of Experimental Neuroscience, 12: 1–4 doi:10.1177/1179069518800508
39. Petri G., Expert P., Turkheimer F., Carhart–Harris R. et al. (2014). Homological scaffolds of brain functional networks. Journal of the Royal Society Interface, 11: 20140873 doi:10.1098/rsif.2014.0873
40. Puig M. V., Gulledge A. T. (2011). Serotonin and prefrontal cortex function: neurons, networks, and circuits. Molecular Neurobiology, 44: 449–464 doi:10.1007/s12035–011–8214–0
41. Santos R. G., Landeira–Fernandez J., Strassman R. J., Motta V. et al. (2007). Effects of ayahuasca on
psychometric measures of anxiety, panic–like and hopelessness in Santo Daime members. Journal of Ethnopharmacology, 112: 507–513 doi:10.1016/j.jep.2007.04.012
42. Sewell R. A., Halpern J. H., Pope H. G. (2006). Response of cluster headache to psilocybin and LSD.
Neurology, 27;66: 1920–1922 doi:10.1212/01.wnl.0000219761.05466.43
43. Simão A. Y., Gonçalves J., Duarte A. P., Barroso M. et al., (2019). Toxicological Aspects and Determination of the Main Components of Ayahuasca: A Critical Review. Medicines, 6, 106 doi:10.3390/medicines6040106
44. Tilakaratne N., Friedman E. (1996). Genomic responses to 5–HT1A or 5–HT2A/2C receptor activation is
differentially regulated in four regions of rat brain. European Journal of Pharmacology, 307: 211–217
doi:10.1016/0014–2999(96)00233–6
45. Vaidya V. A., Marek G. J., Aghajanian G. K., Duman R. S. (1997). 5–HT2A receptor–mediated regulation
of brain–derived neurotrophic factor mRNA in the hippocampus and the neocortex. The Journal of Neuroscience, 15;17: 2785–2795 doi: 10.1523/JNEUROSCI.17–08–02785
46. Vollenweider F. X., Kometer M. (2010). The neurobiology of psychedelic drugs: implications for the treatment of mood disorders. Nature Reviews Neuroscience, 11: 642–651 doi:10.1038/nrn2884
47. Yensen R. (1985). LSD and Psychotherapy. Journal of Psychoactive Drugs, 17: 267–278 doi:10.1080/02
791072.1985.10524331
Mgr inż. Monika Herian, Instytut Farmakologii im. Jerzego Maja Polskiej Akademii Nauk, Zakład Farmakologii, Zespół II, Kraków. E-mail: herian@if-pan.krakow.pl








Komentarze
Bardzo ładny artykuł tylko jak można było na końcu nazwać pochodne LSD "psychodysleptykami" to nie wiem. xP