Muchomor czerwony, Amanita muscaria, oraz muchomor plamisty, A. pantherina są gatunkami wywołującymi zatrucie nazywane 'pantherina-muscaria'.
Przypadki zatrucia są czasami przypadkowe i wtedy głównie wywołane przez A. pantherina, bowiem grzyba tego można pomylić z innymi gatunkami; od czasu do czasu jednak spożywa się A. muscaria w celach rozrywkowych, dla wywołania tego typu zatrucia. Wspomniano w literaturze jedynie bardzo rzadkie zatrucia śmiertelne powyższymi grzybami. Cechą charakterystyczną takiej intokskacji są dysfunkcje centralnego układu nerwowego. Poniższy artykuł opisuje pewne interesujące właściwości tychże grzybów: medyczne, chemiczne, farmakologiczne, historyczne i fitogeograficzne; podejmuje się również syntezy obecnej wiedzy w tej materii. Artykuł kładzie jednak nacisk na biochemiczne właściwości substancji zawartych w grzybach.
Szczegółowe dane mikologiczne A. muscaria i A. pantherina opisano w 1983 (Moser). Kapelusz A. muscaria dorasta do 50 cm średnicy, jest koloru od jasno czerwonego, przez pomarańczowy, do pomarańczowo-żółtego; posiada charakterystyczne białe plamki. Wiele odmian A. muscaria posiada charakterystyczne crassospory (Tulloss & Halling 1997). Gatunków tych nie sposób pomylić z innymi, z wyjątkiem jadalnego A. caesarea (muchomor cesarski). A. pantherina nazywany jest 'panther cap', 'panther Amanita', 'panther agaric' (Am. Północna), 'pantherschwamm', 'krotenschwamm' (Niemcy), 'tignosa' (Włochy), 'pantera', 'pixaca', 'hongo loco', 'hongo malo' (Am. Łacińska) oraz 'amanita panthere' (Francja). Kapelusz A. pantherina ma 5-10 cm średnicy i jest koloru szarego, przez szaro-brązowy, do szaro-żółtego; w trakcie dojrzewania jaśnieje. Podobnie jak A. muscaria, również m. plamisty posiada białe plamki. Kilka zatruć A. pantherina zdarzyło się omyłkowo uznając go za jadalny A. rubescens lub A. spissa. Opisywane gatunki muchomora występują prawie na wszystkich kontynentach, rosnąc w zrzucajacych liście lasach, głównie w bukowych i brzozowych, choć występują również i w lasach iglastych. Inne, podobne gatunki mogą również produkować toksyny zawarte w A. muscaria i A. pantherina; gatunkami tymi są A. regalis i A. strobiliformis (syn. A. solitaria aut.). Odnotowano kilka przypadków podobnego typu zatruć muchomorami z gatunków A. gemmata (syn. A. junquillera), A. crenulata oraz A. cothurnata, lecz nadal ich rzekoma toksyczność wydaje się sporna. Sugeruje się, że zawartość toksyn zależy od miejsca zbioru, na co wskazuje fakt, że pomiędzy poszczególnymi podgatunkami istnieją zmiany składu.
Objawy zatrucia
Zatrucie wywołane Amanita muscaria i A. pantherina nazywa się "mikoatropinowym", bowiem symptomy są podobne do tych wywołanych przez rośliny zawierające atropinę - takie jak Datura stramonium, Atropa belladonna oraz Hyosciamus niger, lecz należy mieć na uwadze, że alkaloidy tropanowe w tychże grzybach nie występują.
Chronosymptomatologia jest zmienna w zależności od podmiotu, zależna od celów spożycia grzyba - obrządków/rytuałów, eksperymentów na samym sobie, czy przypadkowego zatrucia. Przy rytuałach, zatruta osoba (np. szaman) próbuje wywołać właściwy - autosugestywny - stan umysłu. Nie osiąga on całkowitego delirium, a zawarte w grzybach związki poprawiają jego intelekt, sposób rozumowania. Efekty wywołane grzybami w dużym stopniu zależą od podłoża socjokulturowego i nastawienia uczestników spożywających grzyby, czy obecnych przy tej czynności - tzw. set & setting.
W większości przypadków zatrucia, praktycznie po 24 godzinach nie odczuwa się już efektów działania toksyn, nie występują też zauważalne następstwa. W przeciwieństwie do objawów zatrucia grzybami rodzaju Cortinarius, działanie muchomora rozpoczyna się po krótkim opóźnieniu, podobnie jak w zatruciach grzybami z rodzaju Coprinus. Do wywołania efektów psychotropowych, w większości przypadków wystarcza jeden kapelusz, czy szklanka smażonych grzybów.
Efekty pojawiają się po 30 min. do 2 godz. po spożyciu. Występują wtedy: stan zmieszania, zawroty głowy, zmęczenie, estezja (hiperwrażliwość) wzrokowa i słuchowa, zaburzenia postrzegania przestrzeni i brak poczucia upływu czasu; po spożyciu pewnych środków uspokajających, efekty wzmacniają się(!). Nie odnotowano postaw agresywnych (pomimo hipotezy o spożywaniu muchomora przez Wikingów przed walkami w celu wywołania "szału"). Wspominano o suchości w jamie ustnej i mydrazji (rozszerzeniu źrenic). Po około dwóch godzinach od podania często następuje drzemka z barwnymi snami. Głęboki sen, nastepujący po ok. 8 godzinach jest ostatnim objawem stanu zatrucia. Dolegliwości ze strony układu pokarmowego (wymioty) nie zdarzają się przy każdym zatruciu, dlatego nie można uznać ich za objaw charakterystyczny tegoż stanu. Nie odnotowano uszkodzeń organów wewnętrznych, chociaż związek aktywny zawarty w grzybach może indukować uszkodzenie mózgu in vivo, o czym dalej). Regularna konsumpcja grzybów prawdopodobnie będzie szkodliwa dla zdrowia, pomimo braku wyraźnych następstw (szczegóły - również w dalszej części tekstu). U gryzoni, którym podawano kwas ibotenowy i muscymol (związki aktywne w/w grzybów) wykryto pewne uszkodzenia mózgu. Odnotowano również zatrucia grzybami u psów - objawy podobne były do tych wystepujących przy zatruciu u człowieka.
Efekty i siła działania grzybów są związane z czasem ich zbiorów: te zebrane we wrześniu mają słabsze właściwości narkotyczne i wizyjne oraz częściej wywołują nudności, w porównaniu z grzybami zebranymi w sierpniu.
Leczenie zatrucia
Choć efekty działania grzyba ustępują w ciągu 24 godzin, które można wykorzystać w celach m.in. samopoznania, a ewentualne nieprzyjemne efekty zatrucia często wywoływane są przez nieodpowiednie otoczenie i nastawienie to pomijając to - dla upartych, chcących jak najszybciej osiągnąc codzienny stan świadomości - właściwym jest leczenie objawowe. Usunięcie substancji toksycznych z przewodu pokarmowego przez wywołanie wymiotów (np. podając syrop ipekakuany), płukanie żołądka lub podanie węgla aktywnego i środków przeczyszczających, najlepiej na oddziale intensywnej opieki medycznej (teraz warto się zastanowić, czy nie lepiej w takich przypadkach poszukać otuchy u bliskiej osoby, posłuchać kojącej muzyki, porozmyślać nad Wszechświatem niż dzwonić po pogotowie, by resztę tripa spędzić na płukaniu żołądka w zimnej, jasnej sali, pełnej nieznanych osób). Działanie aktywnych składników, kwasu ibotenowego i muscymolu podobne jest do działania atropiny; w związku z powyższym, podawanie atropiny jako antidotum jest niewskazane. Fizostygmina (eseryna), inhibitor cholinoesterazy, jest polecana do neutralizacji efektów zatrucia atropiną i podobnymi lekami antymuskarynowymi. Dawka dożylna dla dorosłych i młodzieży wynosi 1-2mg, powtarzana w razie potrzeby; lek ten wykorzystano z powodzeniem również w przypadkach weterynaryjnych. Przy wystąpieniu konwulsji podaje się środki uspokajające, jak diazepam czy klonazepam, doustnie lub dożylnie, sugerowano również fenobarbitan. Z drugiej strony jednak, diazepam podejrzewa się o wzmacnianie działania muscymolu. W przeciwieństwie do pewnych przekonań, gotowanie muchomorów nie zmniejsza znacząco toksyczności, co pokazuje, że związki aktywne nie są wrażliwe na temperaturę.
Status prawny
Około 12 gatunków trujących grzybów spożywanych jest w celach rozrywkowych, rzadko jednak jest to Amanita muscaria. Prawo włoskie zakazało użycia psylocybiny, psylocyny i A. muscaria ('Stampa alternativa'). Jakkolwiek, w Europie zainteresowanie tymi środkami jest mniejsze niż w Ameryce Północnej, gdzie prawo zakazuje ich użycia - co może nasuwać myśl, że to co zakazane jest bardziej kuszące. Pomimo tego, spożycie A. muscaria, nawet w Europie, wciąż wzrasta. W pewnych krajach posiadanie grzybów halucynogennych nie jest nielegalne, w przeciwieństwie do posiadania oczyszczonych substancji aktywnych, czy pochodnych. Obecne europejskie ustawodawstwo skupia uwagę głównie na Psilocybe semilanceata, i - w mniejszym zakresie - na A. muscaria (Festi, 1985).
Substancje zwarte w muchomorach
Poniżej opiszemy związki aktywne, pigmenty kapelusza i pozostałe, niepospolite związki, zawarte w muchomorze. Co może być dla niektórych ciekawe, większość wytwarzanych przez muchomor substancji jest chemicznie i biogenetycznie powiązana wspólnym fragmentem struktury (Eugster 1969).
Związki psychoaktywne
Mimo, że składniki grzyba zostały gruntownie przebadane, pozostało kilka szczegółów do wyjaśnienia, m.in. sprawa wpływu sposobu przyrządzania grzyba na właściwości fizykochemiczne związków aktywnych. Dla przykładu, meksykanie spożywją owocniki Amanita muscaria bez skórki, którą wcześniej oddzielają; wylewają również wodę, w której muchomory były gotowane (Perez-Silva & Herrera-Suarez 1991). We Włoszech, po zagotowaniu i odlaniu nadmiaru wody, grzyby konserwuje się w solance do czasu spożycia (Festi 1985). W Ameryce Północnej zdejmuje się czerwoną skórkę i pozostawia do wyschnięcia, po czym się ją pali (Ott 1978). Powyższe sposoby przyrządzania powodują, że spora część rozpuszczalnych w wodzie związków aktywnych jest bezpowrotnie usuwana.
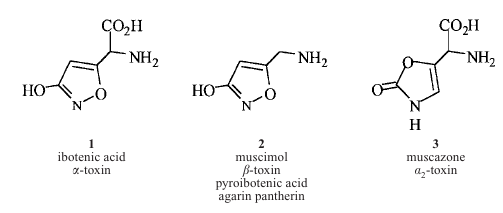
Przyjmuje się, że aktywnymi związkami są muscymol i kwas ibotenowy (choć podejrzewano również inne związki). Związki te są pochodnymi izoksazolu: kwas ibotenowy (od 'iboten-gu-take', japońska nazwa A. strobiliformis; wcześniej nazywany był premuscymolem), oraz produkt jego dekarboksylacji - muscymol - wykryto jedynie w A. muscaria oraz A. pantherina.
Kwas ibotenowy (pantherin, agarin), kwas alfa-amino-3-hydroksy-5-isoksazolooctowy jest bezbarwnym, dobrze rozpuszczalnym w zimnej wodzie krystalicznym związkiem (C5H6N2O4, m. mol 158.11, t.t. 150-152C z rozkładem). Dehydratacja prowadzi do dekarboksylacji, w której powstaje muscymolu, co sugerowało by, że spożywając gotowane grzyby, lub nawet po procesie trawienia, jedynym związkiem docierającym do mózgu i odpowiedzialnym za efekty psychotropowe jest muscymol. Czerwona skóra kapelusza i żółty miąższ poniżej zawiera największe ilości w/w substancji, co tłumaczyło by praktyki jej zdejmowania.
Muscymol, 5-(aminometylo)-3-hydoksyizoksazol 2, wyizolowany z A. muscaria, jest bezbarwną, dobrze rozpuszczalną w wodzie substancją krystaliczną (C4H6N2O2, m. mol. 114.10, t.t. 175 C z rozkładem). W 1985 odkryto, że budowa panteryny, wyodrębnionej z A. pantherina, jest bardzo podobna do budowy "agaryny" (kwasu ibotenowego) (a więc odkryto, że oba grzyby zawierają ten sam związek).
Muskazon, kwas alfa-amino-2,3,-dihydro-2-okso-5-oksazolooctowy, jest bezbarwnym ciałem krystalicznym, również wyodrębnionym z omawianych grzybów; jego struktura została potwierdzona przez syntezę. Tenże laktam powstaje w wyniku foto-przegrupowania muscymolu i wytwarza się głównie podczas procesu analizy składników muchomora. Muskazon wywołuje słabe efekty farmakologiczne w porównaniu z poprzednimi substancjami. Co ciekawe, podobna w budowie do muscymolu cykloseryna (myxomycin, seromycin, D-4-amino-3-isoksazolidon) jest związkiem przeciwbakteryjnym i tuberkulostatycznym. Wiadomo, że działa ona na c.u.n. (jednak z większym opóźnieniem) wywołując senność, zamieszanie, nerwowość.
Po rozwiązaniu budowy związków aktywnych, otrzymano ich tio-pochodne, które okazały się jeszcze silniejszymi inhibitorami wychwytu GABA. Preparatykę w skali gramowej przeprowadzono przy użyciu regiospecyficznej 1,3-dipolarnej cykloaddycji/eliminacji. Otrzymano też tiomuscymol, którego właściwości wiążące są na tyle silne, że wypierają GABA z receptora.
Ilości muscymolu wykryte w próbkach grzybów wynosiły 0.19% suchej masy A. muscaria i 0.3% suchej masy A. pantherina. Stijve (1981) pokazał, że ilości muskaryny są bardzo małe (0.009% u A. muscaria i mniej niż 0.0005% u A. pantherina). Dla porównania, pewne gatunku Inocybe i Clitocybe, odpowiedzialne za typowe objawy zatrucia muskaryną, zawierają tę substancję w ilości 0.1-0.3% suchej masy.
Największe ilości k. ibotenowego i muscymolu wykryto w żółtym miąższu pod skórką, k. ibotenowego: 548 nmola/g świeżej masy i muscymolu: 366 nmol/g świeżej masy (Gore & Jordan 1982). Ekstrakty grzybów ekstrahowane kwasem octowym zawierały muscymol na poziomie 40 ppm, pokazując, że kwas ibotenowy jest głównym składnikiem grzybów, zaś muscymol jest związkiem psychoaktywnym powstającym przez dekarboksylację podczas przygotowywania muchomora do zjedzenia. Stosując jonową HPLC odkryto, że ilości obu związków były wyższe w kapeluszu niż trzonie; średnia wartość dla k. ibotenowego i muscymolu to, kolejno (świeża masa) 990 mg/kg (kapelusz), 230mg/kg (trzon) i 380mg/kg (kapelusz) i 80mg/kg (trzon). Średniej wielkości świeży owocnik A. muscaria (60-70g) zawiera do 70mg k. ibotenowego.
Inne związki czynne
(-)-R-4-hydroksy-pirolidon-(2), który strukturalnie jest podobny do kwasu ibotenowego i muscymolu, wykryto w Amanita muscaria w 1969. Tego typu szkielet zwykle wykazuje silną aktywność biologiczną przeciwko bakteriom i innym grzybom (np. aureothrycin, equisetin). Dzięki wykryciu tego związku można zasugerować biogenezę k. ibotenowego, muscymolu i muskazonu. Prawdopodobnie wszystkie pochodzą od tego samego prekursora, kwasu beta-hydroksyglutaminowego, którego cyklizacja i dekarboksylacja prowadzi do w/w związków.
Kwasy stizolobowy i stilozobinowy, znane ze Stizolobium hasjoo znaleziono w A. pantherina, lecz nie w A. muscaria; małe ich ilości wykryto w A. gemmata. Kwas stizolobowy, a w mniejszym stopniu również kwas stizolobinowy, wykazuje działanie pobudzające w wyizolowanych rdzeniach kręgowych szczurów. Badania biosyntetyczne pokazały, że oba te aminokwasy pochodzą od 3,4-dihydroksyfenyloetyloalaniny (DOPA).
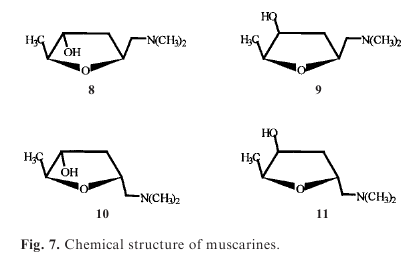
Przez długi czas uważano, że aktywną substancją w A. muscaria jest muskaryna, sugerując się jej działaniem na centralny układ nerwowy. Później to zdyskredytowano, acz pomimo tego, część publikacji wciąż źle przypisuje muskarynie udział w działaniu, chociaż kilka analiz wykazało, że związek ten (występujący jedynie w minimalnych ilościach w Amanita'ch) nie jest odpowiedzialny za efekty zatrucia 'pantherina-muscaria' (należy jednak pamiętać, że sama muskaryna jest silną trucizną, po której następuje raczej zgon niż kontakt z wyższymi jaźniami). Zaobserwowano występowanie muskaryny w A. muscaria w małych ilościach (0,0002-0,0003%). W porównaniu z Inocybe spp., czy Clitocybe spp. można ją uważać za związek wyst. w ilościach śladowych (0.43% w Inocybe subdestricta, do 0.15% w Clitocybe dealbata). Oba gatunki Amanita nie powinny wykazywać efektów zatrucia muskarynowego, pomijając przypadki nadmiernego ich spożycia.
Obecność w A. muscaria amatoksyn i fallotoksyn, typowych toksyn A. phalloides (muchomora sromotnikowego), początkowo wykluczono, aczkolwiek wysoce wrażliwe metody detekcji wykazały ich ślady. Innym prawdopodobnym związkiem aktywnym, zaproponowoanym przez Waser'a w 1967 była bufotenina (5-hydroksy-N,N-dimetylotryptamina), lecz występowania w amanitach halucynogennych pochodnych indolowych, takich jak często spekulowanej psylocybiny, nie potwierdzono.
Pigmenty
Musarufina jest podstawowym pigmentem opisywanych grzybów; prawdopodobnie jest ona pochodną terfenylochinonu, lecz wysiłki różnych grup badawczych tego nie potwierdziły.
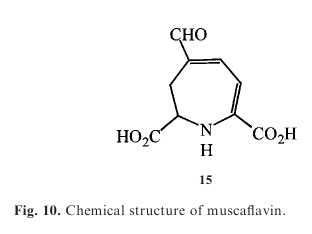
Musso zaproponował całkiem nową strukturę żółtego pigmentu, muscaflavinę; wyniki jego dociekań potwierdzono przez ścieżkę biosyntetyczną, która uwzględnia utlenienie L-DOPY, a następnie cyklizację, które prowadzą do muscaflaviny, kwasu betalamowego, k. stizolobowego, k. stizolobinowego. Strukturę potwierdzono przez syntezę. Muscaflavinę wykryto również w czerwonych owocnikach gatunku Hygrocybe.
Inne
Zawarta w muchomorze 1,3-dioleina, diester glicerolu i kwasu oleinowego wykazuje działanie zwabiające muchy.
Wiadomym jest, że grzyby te akumulują metale. A. muscaria może akumulować wanad w ilości do 200ppm (30 razy więcej niż w żywych organizmach). Izolację, wyznaczanie struktury i syntezę jasnoniebieskiego kompleksu wanadu, amawadyny przeprowadzono w 1986. Wykryto też nietypowo wysoką zawartość selenu (do 17.8 ppm) i metali ciężkich: kadmu 13.9, kobaltu 2.6, chromu 1.7, ołowiu 33.3, rtęci 61.3, niklu 7.5 ppm.
Sposób działania toksyn
Działanie in vivo kwasu ibotenowego i muscymolu
Zmiany biochemiczne następują 30 min. po wstrzyknięciu wodnego ekstraktu A. muscaria, A. pantherina i A. rubrovolvata samcom szczura. Następuje obniżenie aktywności esterazy acetylocholinowej, glikogenu wątrobowego, mocznikowego azotu w krwi, zwiększa się ilość glukozy we krwi, aktywność transaminazy osocza pozostaje niezmieniona. Wartości wracają do standardowych w ciągu 6. godzin. Powyższe dane pokazują, ze zatrucie nie jest poważne i że istotne organy, jak wątroba czy nerki nie są atakowane. Aktywną dawką muscymolu podaną doustnie jest 7,5-10mg, a LD50 (dootrzewniowo) wynosi 2,5mg/kg dla myszy i 3.5mg/kg u szczura. Przy dootrzewniowym i doustnym podaniu muscymolu (4-8mg/kg) i k. ibotenowego (16mg/kg), źrenice myszy ulegają rozszerzeniu. Oba narkotyki indukują działanie anoreksogeniczne u myszy (2-3mg/kg) z uspokojeniem, śpiączką, drganiem mięśni i katalepsją. Narkotyk wytwarza zapis EEG różniący się od wywołanego przez inne substancje halucynogenne, jak LSD czy meskalina - wyglądem EEG przypomina raczej te wywołane przez leki antycholinergiczne, jak atropina i Ditran.
Najbardziej prawdopodobne jest, że po podaniu substancji, niskie pH kwasów żołądkowych powoduje hydrolizę kwasu ibotenowego do muscymolu, który następnie dociera do mózgu lub jest usuwany przez krążenie duże. Pozostałości składników aktywnych w moczu tłumaczą tradycję picia moczu szamana (lub zwierząt, które jadły grzyby) u plemion syberyjskich w celu osiągnięcia stymulacji 'second-hand. Kwas ibotenowy i muscymol pojawiają się w ludzkim moczu godzinę po spożyciu; obserwację te potwierdzono eksperymentalnie u myszy.
Powtarzane iniekcje kwasu ibotenowego indukowały tymczasowe zmiany w czułości receptorów GABA i mogą prowadzi do uszkodzeń w części podstawnej kresomózgowia niszcząc mały procent komórek cholinergicznych; konsekwencją działania in vivo były znaczące i przedłużające się ubytki pamięci i zdolności uczenia się. W przypadku młodych ssaków, muscymol zaburzał również tworzenie się układu noradrenalinowego w hipokampie.
Biochemia pochodnych kwasu ibotenowego
Efekty działania czystego kwasu ibotenowego i muscymolu są podobne, lecz nie identyczne w porównaniu do działania grzybów in toto. Kwas ibotenowy i muscymol należą do wyróżniającej się grupy alkaloidów, pobudzających aminokwasów. Grupa ta zawiera kwas kainowy, kwas domoikowy, kwas tricholomowy, kwas kwiskwalowy, junainę, petaloninę; wszstkie będące naturalnie występującymi aminokwasami.
Kwas ibotenowy i muscymol są konformacyjnie usztywnionymi pochodnymi kwasu glutaminowego i kwasu gamma-aminomasłowego (GABA). W rezultacie, działają one jako neuroprzekaźniki biorące udział w kontroli aktywności neuronalnej w centralnym układzie nerwowym ssaków, działając na neurony rdzenia kręgowego. Kwas ibotenowy działa na receptory kwasu glutaminowego, natomiast muscymol działa na receptory GABA. W przeciwieństwie do kwasu glutaminowego i GABA, kwas ibotenowy i muscymol przechodzi przez barierę krew-mózg.
U kotów obserwowano pobudzające działanie kwasu ibotenowego i depresyjne działanie muscymolu.
Kwas glutaminowy jest głównym pobudzającym neuroprzekaźnikiem w centralnym układzie nerwowym ssaków, a jego receptory są odpowiedzialne za zaburzenia neurologiczne, takie jak epilepsja czy pląsawica Huntingtona. Receptory inhibitorowe glutaminianu (IGluRs) stanowią grupę białkowych kanałów jonowych równoważnych z receptorami glicynowymi i GABA. Kwas ibotenowy działa na IGluRs (Cleland 1996). AMPA, syntetyczny analog kwasu ibotenowego jest bardziej efektywnym i specyfycznym agonistą receptora glutaminianu niż cząsteczka k. ibotenowego. Injekcje dootrzewne muscymolu i kwasu ibotenowego powodują wzrost serotoniny i dopaminy w mózgu myszy i szczurów, co może objawić się brakiem apetytu i rozszerzeniem źrenic. Toksyny muchomora silnie wiążą się z receptorami gamma-aminomaślanu (GABA). Co więcej, są one również inhibitorami neuronalnego i glejowatego wychwytu GABA oraz substratem dla metabolizującego GABA enzymu - transaminazy GABA. Po odkryciu zależności między stężeniem GABA, a epilepsją, oraz wiedząc, że muscymol jest agonistą receptorów GABA, otrzymano bardziej lipofilne bioizosteryki muscymolu, jak np. Tiagabine, który sprzedawany był jako lek na epilepsję, "Gabatril".
ETNOMIKOLOGIA
Amanita w kulturze człowieka
Spośród wszystkich gatunków grzybów, muchomor od dawna jest grzybem cieszącym się największym zainteresowaniem; był ucieleśnieniem terminu "grzyb" i prawdopodobnie jest najczęściej rysowanym gatunkiem. Pomimo złej reputacji, grzyb ten dzięki zachwycającemu wyglądowi jest najczęściej stosowanym piktogramem dla dzikich grzybów. Używa się go na ilustracjach do bajek i w kreskówkach, dekoruje się jego symbolem choinki świąteczne, ciasta, czy nawet tatuuje. Wykorzystywali go szamani, czarownicy, wiedźmy, jak i inni kapłani różnorakich grup etnicznych, oddalonych od siebie kulturalnie i geograficznie. Kapłani, próbując leczyć ludzi używali grzyba w rytuałach religijnych. Wasson (1959) przekonująco pokazał, że grzyb ten był "somą" u starożytnych plemion, Ariów. Pojęcie to określało "roślinę" wydzielającą sok przy wyciskaniu, który następnie filtrowano i stosowano jako boski środek odurzający. Wasson podawał kilka fragmentów Rigwed, które opisywały, że starożytni często spożywali grzyby dla ich właściwości psychoaktywnych. Poza różnymi symbolami, które mogą odnosić się do A. muscaria i pochodzenia z tradycji północnej i południowej Azji, dostrzega się również pewne odniesienia do grzyba w mitach buddyjskich. Grzyby te pojawiały się też w tradycji Germańskiej, związane były z bogiem Odynem. Kilka publikacji utrzymuje, że Chrześcijaństwo pochodzi od kultu A. muscaria. Podobno Jezus został obdarzony energią grzyba (Allegro 1970, 1971), lecz inni badacze biblii i religii zdyskredytowali tę tezę (King 1970). Solidne źródła podają, że plemiona Ostjaków i Mansów zachodniej Syberii, oraz Itelmeni, Korjakowie, Czukczowie z Syberii wschodniej, wciąż używają A. muscaria w obrządkach szamańskich. Jakkowiek, w przeciwieństwie do grzybów halucynogennych (głównie gatunków Psilocybe) używanych w kulturze mezoamerykańskiej, muchomory nie są obiektem religijnej i rytualnej czci.
Malowidła, freski i dane archeologiczne, np. malunki naścienne, rzeźby w drewnie, czy posągi sugerowały, że właściwości psychotropowe Amanita znane są od czasów starożytnych, a ich właściwości terapeutyczne i wykorzystanie w rytualnych obrządkach znane było na całym świecie. Na skalnych malowidłach z Sahary da się zauważyć muchomory, najprawdopodobniej A. muscaria; pracę tę datuje się na okres Paleolitu, 9000-7000 r. p.n.e.
Nazwa grzyba
Nazwa gatunku jako "muchomor" (fly agaric, bug agaric) jest, co ciekawe, taka sama na całym świecie: 'amanite tue-mouche' (Francja), 'Flegenpilz' (Niemcy), Muchomor (Rosja), 'moscario' (Włochy), 'hongo mosquero', 'hongo matamoscas' (Hiszpania). Nazwa Amanita strobiliformis w japońskim brzmi 'haetorimodashi', zabójca much. Na początku XIX wieku, Atkinson (1901) wspomniał o przygotowaniu grzyba do zabijania much, co dziś zostało zweryfikowane doświadczeniem pokazującym, że muchy nie zdychają, a jedynie zapadają w przemijającą śpiączkę, po której odlatują. Jakkolwiek, pewne doświadczenia pokazały, że gatunki Amanita zatrzymują wzrost larw Drosophila melanogaster karmionych sproszkowanymi owocnikami.
Zawarta w nazwie "mucha" może być jednak tłumaczona inaczej, bowiem już od czasów starożytnych muchę kojarzono z szaleństwem i nadprzyrodzonymi mocami. W Średniowieczu wierzono, że muchy i inne insekty mogą penetrować głowę i wywoływać choroby psychiczne. W Europie, pewne terminy określające te grzyby kojarzą się z szaleństwem, np. 'Narrensch-wamm' (Niemcy), 'oriol fol' (Katalonia), 'mjioulo folo' (dialekt tuluzyjski), 'coucourlo foulo' (język d'oc) i 'ovolo matto' (północne Włochy) (Festi 1985). Inny przykład występuje w Biblii: Belzebub, oznacza 'Pan much' i jest synonimem fałszywego boga czczonego przez odurzonych. Najprawdopodobniej nazwa A. muscaria pochodzi od 'grzyb much' ponieważ jest w stanie indukować boskość lub piekło, stany podobne do tych, które wywoływały muchy penetrujące ludzkie mózgi.





Komentarze
O kurwa... Świetny artykuł!!!
Super artykuł, szczególnie pod względem chemicznym itp., co się chwali!
W pobliskim lasku potykałem się o nie, szukając grzybów na jajecznice. Co jak co, ale nie zjadł bym gówna. Większość użytkowników hypka ma mocno nadwyrężone wątroby i inne podroby. Poza tym na wiki wyczytałem coś o śmiertelności 2-5% przy zatruciu. Ale życzę miłych halunów.
Trzeba wszystko robić z głową i po to są takie artykuły. Też gdzieś wyczytałem, że w tym roku odnotowano ponad 900 zatruć, z tego 2 ciężkie, a w jednym przypadku zgon i nie m. czerwonym tylko sromotnikowym. Aha, koleś podobno cały miskę sromotników z ziemniakami wmłócił. Podejrzewam, że gdyby najadł się tyle samo maślaków też by nie miał lekko
świetny tekst, bardzo dziękuję za tłumaczenie i udostępnienie go tutaj :)
Na takich tekstach hyperreal zyskuje najbardziej.. świetnie.
serdecznie dziękujemy :-) :-)
jeśli macie jakieś propozycje co warto by przelać na polski, dajcie znać (najlepiej tu)
Pięknie Dziękuję :)
Zapraszamy do wzięcia udziału w badaniu duchowości osób zażywających muchomora czerwonego (Amanita Muscaria) 🍄
Jest ono skierowane do osób pełnoletnich.
Są one realizowane przez młodych naukowców przy Instytucie Pedagogiki Uniwersytetu Gdańskiego, a wyniki posłużą do opracowania wniosków o charakterze naukowym.
Prosimy również o udostępnienie linku do badania 😊
https://forms.office.com/r/6jwEd0h1p1