Trip report przeniesiony z forum hyperreal.info.
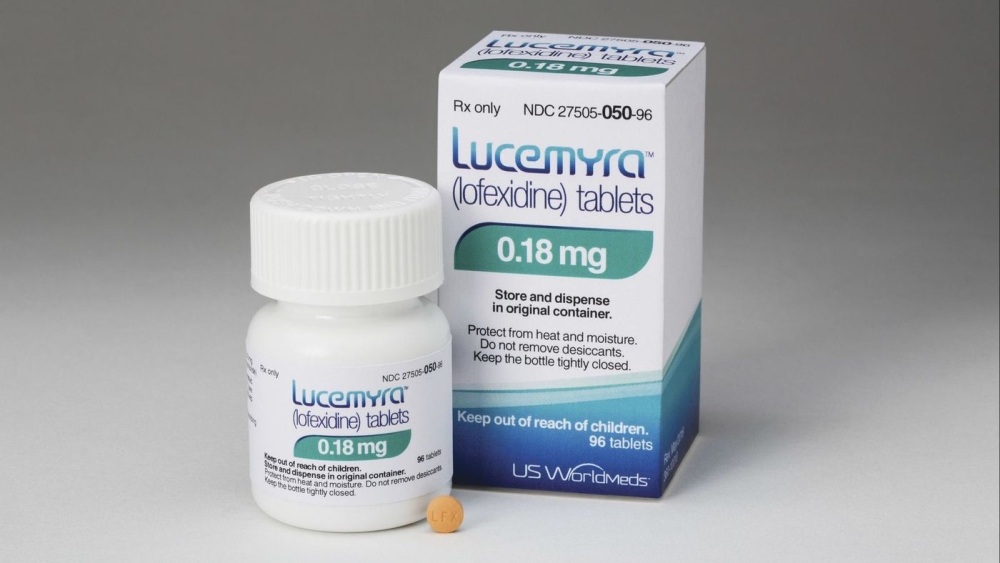
Chlorowodorek lofeksydyny to pierwszy lek ze wskazaniem do złagodzenia objawów nagłego odstawienia opioidów u osób dorosłych, zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
Chlorowodorek lofeksydyny to pierwszy lek ze wskazaniem do złagodzenia objawów nagłego odstawienia opioidów u osób dorosłych, zatwierdzony przez amerykańską Agencję ds. Żywności i Leków. FDA zastrzega, że może być stosowany tylko przez 14 dni, jako element szerszego, długoterminowego planu leczenia zaburzeń związanych ze stosowaniem leków opioidowych (OUD).
Odstawienie opioidowych leków przeciwbólowych może powodować niepokój, pobudzenie, problemy ze snem, skurcze żołądka, bóle mięśniowe, bicie serca, katar, poty, uczucie chłodu, nudności, wymioty, biegunkę, a także objawy podobne do głodu narkotykowego. Mogą one wystąpić po nagłym odstawieniu lub zmniejszeniu dawki leków opioidowych, i to zarówno u pacjentów z objawami uzależnienia od nich, jak również u pacjentów, którzy stosowali je zgodnie z zaleceniami lekarskimi.
W USA u pacjentów przestrzegających zaleceń odstawianie opioidów zwykle odbywa się poprzez powolne zmniejszanie dawki leku, co ma na celu uniknięcie lub zmniejszenie skutków odstawienia, pozwalając jednocześnie organizmowi pacjenta przystosować się do braku leku. W przypadku pacjentów z objawami uzależnienia od danego opiatu, zwykle zastępuje się go innym lekiem opioidowym, a następnie stopniowo zmniejsza jego dawkę lub przechodzi na terapię podtrzymującą - metadonem, buprenorfiną, naltreksonem albo dostepnymi bez recepty lekami, których działanie ukierunkowane jest na konkretne objawy OUD, np. przeciwbólowymi lub gastrycznymi.
Zatwierdzony przez FDA chlorowodorek lofeksydyny (Lucemyra) jest doustnym, selektywnym agonistą receptora alfa 2-adrenergicznego, który zmniejsza uwalnianie norepinefryny. Uważa się, że jej działanie w autonomicznym układzie nerwowym odgrywa rolę w wielu objawach odstawienia opioidów.
Bezpieczeństwo i skuteczność Lucemyry potwierdzono w dwóch randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach klinicznych z udziałem 866 osób dorosłych osób, które były uzależnione od opioidów i u których nagle odstawiono te leki. Do najczęstszych działań niepożądanych związanych ze stosowaniem tego produktu należały: niskie ciśnienie krwi, bradykardia, senność, sedacja i zawroty głowy. W kilku przypadkach Lucemyra spowodowała omdlenie. Może również zwiększać ryzyko nieprawidłowych rytmów serca. Po jej odstawieniu pacjenci mogą odczuwać wyraźny wzrost ciśnienia krwi.
"Opracowujemy nowe wytyczne, aby pomóc przyspieszyć opracowanie lepszych metod leczenia, w tym takich, które pomagają w radzeniu sobie z objawami odstawienia opioidów. Wiemy, że fizyczne objawy odstawienia opioidów mogą być jedną z największych barier dla pacjentów szukających pomocy z powodu uzależnienia od opioidów. A ci, którzy szukają pomocy, mogą z niej zrezygnować z powodu ciągłych objawów odstawienia” – powiedział Scott Gottlieb, komisarz FDA.
Chłodny listopadowy dzień, ulice i środki komunikacji miejskiej Trójmiasta, zimny i niewygodny garaż na jakimś zadupiu, wspaniały humor w związku ze spotkaniem z moimi ulubionymi ćpunkami ;) Kompania w składzie: ja, Bill, Ironia, McOffsky, Jezus i koleżanka spoza forum - D.
Trip report przeniesiony z forum hyperreal.info.
Doświadczenie : medytacja , łysiczki
Do spożycia ayahuascy przygotowywałem się kilka tygodni , chociaż jak teraz na to patrzę to pierwsze kroki przygotowań zrobiłem juz 3 lata temu . Rytuał zaplanowałem na pierwszego listopada w święto zmarłych i postanowiłem , że zrobię to w nocy w lesie - tak jak robią to szamani w dżungli .
Zaczynam pisać ten artykuł w godzinę po zarzuceniu 20 tablet Avio.........jak na razie bez rezultatu. :{
Czwartek, godz. 23.41. Zastanawiam się czy nie lepiej wyjść na miast i zobaczyć czy ten "lek" naprawdę działa , ale boję
się troszkę, że będąc na jeździe ktoś mi z tulipana w potylice nie przyłoży........zaczekam 15 minut i spadam. Machnę krótki
spacerek i zobaczymy czy świat jeszcze istnieje.Objawy? Lekka senność i znużenie. NIc , czego nie możnaby było się
dowiedzieć z ulotek w opakowaniach.
Przyjemny, słoneczny dzień, wśród znajomych w parku.
W moim krótkim życiu dałem trzy szansę marihuanie. O jedną za dużo.Pierwszy raz wszystko było w porządku, ale za drugim razem miałem bad tripa w takim stopniu że trafiłem na kardiologię.
Przez następne sześć miesięcy brzydziłem się marihuaną.
Pewnego dnia mój kolega T zadzwonił do mnie czy nie mam załatwić czegoś zielonego. Oczywiście będąc dobrym kolegom szybko uruchomiłem znajomości i po 30 minutach miałem materiał w kieszeni. Oczywiście mój dostawca się zmienił od mojej drugiej przygody z marihuaną, pomyślałem że to była jakaś maczanka.